Die polare Atombindung
Viele Salze sind in Wasser gut löslich. Im Kapitel zur Ionenbindung haben wir dies damit erklärt, dass Wasser ein polares Lösungsmittel ist. Hier wird nun erklärt, was dass heißt.
Die Atombindungen im Wassermolekül sind polarisiert, das heißt,
das bindende Elektronenpaar ist nicht jeweils in der Mitte zwischen dem Sauerstoffatom und einem der
Wasserstoffatome, sondern der Sauerstoff zieht es mehr zu sich herüber. Man sagt auch, Sauerstoff
habe eine größere Elektronenaffinität als der andere Bindungspartner, der Wasserstoff.
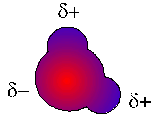 Man bezeichnet diese
geringe Ladungsverschiebung gerne mit einem kleinen griechischen δ+ bzw. δ–,
um zu verdeutlichen, dass es sich nicht um eine vollständige
Elementarladung handelt.
Man bezeichnet diese
geringe Ladungsverschiebung gerne mit einem kleinen griechischen δ+ bzw. δ–,
um zu verdeutlichen, dass es sich nicht um eine vollständige
Elementarladung handelt.
Ein Maß für die unterschiedlichen Elektronenaffinitäten der verschiedenen Elemente ist
die Elektronegativität. Je höher ihr Wert, desto stärker zieht das betreffende Element
Elektronen zu sich herüber. Das Element mit der höchsten Elektronegativität ist das Fluor mit einem
EN-Wert von 4.
Ist die Differenz der EN-Werte zweier Elemente größer als 1,7, dann zieht das elektronegativere
Element die Elektronen ganz zu sich herüber: es liegt eine Ionenbindung vor.
Ist die EN-Differenz geringer, spricht man von einer mehr oder weniger polaren Atombindung.
Bei sehr geringer Differenz spricht man von einer reinen Atombindung.